時(shí)間:

翻譯:華溶應(yīng)用中心
審核:工業(yè)藥劑發(fā)燒友
Doxil?是FDA批準(zhǔn)的一種復(fù)雜靜脈注射多柔比星(DOX)脂質(zhì)體制劑。對(duì)于多柔比星脂質(zhì)體仿制藥,分析DOX的釋放曲線對(duì)于質(zhì)量控制和可比性研究非常重要。然而,尚無可靠的多柔比星脂質(zhì)體標(biāo)準(zhǔn)藥物釋放試驗(yàn)。在本研究中,我們闡述了一種基于USP-4裝置的分析方法,能夠根據(jù)釋放曲線區(qū)分DOX脂質(zhì)體制劑。在37℃的生理?xiàng)l件下,脂質(zhì)體的DOX釋放有限,從而阻礙了測(cè)定方法的建立。向釋放介質(zhì)中添加NH4HCO3有助于DOX釋放,這與添加的鹽濃度成比例,但這會(huì)導(dǎo)致釋放的藥物在流池法裝置中沉淀。在釋放介質(zhì)中加入羥丙基環(huán)糊精 (HP-CD) 可避免DOX沉淀。我們通過改變HP-CD濃度、試驗(yàn)溫度和試驗(yàn)樣品濃度等參數(shù),優(yōu)化了DOX釋放的條件。優(yōu)化的釋放介質(zhì)包括:100mM NH4HCO3、75mM 2-(N-嗎啉代)乙磺酸(MES)和5%(w/v)HP-CD、5%(w/v)蔗糖、0.02%(w/v)NaN3(pH6)。在45℃下進(jìn)行藥物釋放試驗(yàn),優(yōu)化的釋放試驗(yàn)可以區(qū)分不同處方、不同理化性質(zhì)以及通過不同生產(chǎn)工藝制備的DOX脂質(zhì)體制劑,這表明,該分析方法可用于比較DOX仿制藥與創(chuàng)新藥Doxil?的DOX釋放。
Doxil?是一種多柔比星脂質(zhì)體制劑,最初于1995年獲得FDA批準(zhǔn),用于治療不同的惡性腫瘤,如艾滋病相關(guān)的卡波西肉瘤、復(fù)發(fā)性卵巢癌、轉(zhuǎn)移性乳腺癌和多發(fā)性骨髓瘤。Doxil?由美國(guó)強(qiáng)生公司(J&J) 銷售,于2010年失去專利保護(hù)。Doxil?生產(chǎn)高度復(fù)雜,涉及多個(gè)工藝,包括形成多層載體、擠出形成單層脂質(zhì)體、將多柔比星主動(dòng)載入脂質(zhì)體、緩沖液交換/純化、無菌過濾和瓶裝。由于產(chǎn)品的復(fù)雜性,該產(chǎn)品的仿制藥發(fā)展受到限制。2013年,由Sun Pharma(印度)生產(chǎn)的第一款參照Doxil?的仿制藥鹽酸多柔比星脂質(zhì)體注射液(如Doxil?)被美國(guó)FDA批準(zhǔn)進(jìn)口。多項(xiàng)分析測(cè)試以評(píng)估Doxil?及其仿制藥的理化等效性。FDA關(guān)于多柔比星脂質(zhì)體注射液仿制開發(fā)的個(gè)藥指南,強(qiáng)調(diào)體外泄漏測(cè)試“以支持在一系列生理?xiàng)l件下沒有不受控制的泄漏并向腫瘤部位細(xì)胞遞送等效藥物”。與可獲得藥典標(biāo)準(zhǔn)釋放試驗(yàn)的常規(guī)劑型不同,對(duì)于復(fù)雜脂質(zhì)體產(chǎn)品(如Doxil?),目前尚無藥典標(biāo)準(zhǔn)釋放試驗(yàn),因此難以進(jìn)行實(shí)驗(yàn)室間對(duì)比和脂質(zhì)體仿制藥的開發(fā)。因此,非常需要開發(fā)用于檢測(cè)Doxil?等復(fù)雜脂質(zhì)體制劑藥物泄漏的標(biāo)準(zhǔn)釋放試驗(yàn)。
流池法溶出儀近期已用于微粒和脂質(zhì)體制劑的釋放研究,結(jié)果令人鼓舞。因此,我們的目標(biāo)是開發(fā)多柔比星脂質(zhì)體的USP-4體外釋放方法。與傳統(tǒng)的釋放試驗(yàn)(例如透析袋和“取樣和分離”方法)相比,流池法釋放試驗(yàn)用于多柔比星脂質(zhì)體的優(yōu)點(diǎn)包括:(a)使用標(biāo)準(zhǔn)流池法溶出裝置;(b)易于調(diào)節(jié)釋放試驗(yàn)的不同參數(shù)(如溫度、流速和檢測(cè)波長(zhǎng))的能力;(c)在線UV檢測(cè)器連續(xù)自動(dòng)檢測(cè)多柔比星的釋放,無需取樣。總體而言,這些優(yōu)勢(shì)有助于建立穩(wěn)健的釋放試驗(yàn),該試驗(yàn)受操作誤差的影響較小,并且可在多柔比星脂質(zhì)體產(chǎn)品生產(chǎn)商之間輕松轉(zhuǎn)移。
在當(dāng)前研究中,我們開發(fā)了流池法多柔比星脂質(zhì)體釋放試驗(yàn),能夠區(qū)分不同脂質(zhì)體組成以及相同組成但通過不同工藝制備的制劑。在加速條件下,當(dāng)超過70%的藥物在24小時(shí)內(nèi)釋放時(shí),已建立的流池法釋放試驗(yàn)評(píng)估了多柔比星的滲漏。通過優(yōu)化樣品與釋放介質(zhì)的比例、溫度、組成(如緩沖液組分)、氨離子加入量以及多柔比星受體環(huán)糊精的加入量,建立了測(cè)定方法。該方法可用于評(píng)估批與批產(chǎn)品的變異性、在生產(chǎn)工藝或設(shè)備變更后產(chǎn)品質(zhì)量一致性測(cè)試,并為仿制藥處方設(shè)計(jì)提供有用的反饋。它可以在未來用于潛在建立這些制劑的體外釋放行為與體內(nèi)藥代動(dòng)力學(xué)之間的相關(guān)性。
2.1 化學(xué)品和試劑
多柔比星購(gòu)自SHJNJ PharmaTech(中國(guó)上海)和LC實(shí)驗(yàn)室(Woburn,MA)。脂質(zhì)組分:氫化大豆磷脂酰膽堿 (HSPC);1-棕櫚酰基-2-油酰基-Sn-甘油-3-磷酸膽堿 (POPC);1,2-二硬脂酰-Sn-甘油-3-磷酸乙醇胺-N-氨基(聚乙二醇)-2000 銨鹽(DSPE-PEG2000)購(gòu)自Lipoid(紐約),膽固醇購(gòu)自AvantiPolar Lipids(Alabaster)。Doxil?是從密歇根大學(xué)醫(yī)院藥房購(gòu)買。β-環(huán)糊精(β-CD)和羥丙基環(huán)糊精(HP-CD)由Roquette Pharma贈(zèng)送。此外,HP-CD、β-CD和β-CD購(gòu)自SHJNJ Pharmatech(中國(guó)上海)。NH4HCO3從Sigma購(gòu)買。Float-a-lyzer?(截留分子量為10-300kDa)透析管購(gòu)自Spectrum Laboratories。蔗糖購(gòu)自Fluka。所有其他試劑均為分析級(jí),從Sigma購(gòu)買。為確保定量分析和釋放試驗(yàn)的準(zhǔn)確性,本研究中使用的所有緩沖液在使用前立即新鮮制備。
2.2 方法
2.2.1 多柔比星脂質(zhì)體的制備
將HSPC、膽固醇和DSPE-PEG2000以3:1:1的重量比(表I)溶解在1mL乙醇(EtOH)中,制備脂質(zhì)溶液。對(duì)于POPC -脂質(zhì)體制備,用等量POPC取代HSPC(表I)。將混合物加熱至65℃,直至所有固體完全溶解。通過向硫酸銨溶液中加入脂質(zhì)形成多層脂質(zhì)體(MLVs)(脂質(zhì)加成法)。具體而言,將脂質(zhì)/乙醇溶液倒入65℃攪拌的0.25M 硫酸銨溶液(L-DOXp)中,或高壓注入65℃攪拌的0.25M 硫酸銨溶液(L-DOXi)中,并在相同溫度下攪拌十分鐘,然后擠出。隨后以相同的方式處理MLVs以制備L-DOX。簡(jiǎn)言之,將Lipex擠出機(jī)(Northern Lipids, Burnaby, BC, CA)加熱至65℃,并在添加MLVs之前用0.25M 硫酸銨溶液沖洗。在擠出機(jī)中加熱MLVs 1分鐘后,壓力增加,直到出口管保持恒定流量。在室溫下,通過動(dòng)態(tài)光散射(DLS, ZetaSizer 3000HSa)測(cè)量,重復(fù)擠出大約六次,直到脂質(zhì)體平均直徑在85-90nm之間且多分散度(PDI)小于0.1。H-DOX通過與L-DOXp相同的方式形成MLVs,然后使用微射流機(jī)((Microfluidics M-110P, Microfluidics, Westwood, MA)進(jìn)行高壓均質(zhì)化,特別是在10000-15000psi下進(jìn)行兩次均質(zhì)化。通過透析法(4℃)在5 mM HEPES,10% w/v蔗糖(pH 6.5)條件下將脂質(zhì)體從硫酸銨中分離。
為了將多柔比星裝入脂質(zhì)體中,將鹽酸多柔比星(DOX?HCl)粉末以10mg DOX?HCl/mL的濃度溶解在5 mM HEPES,10% w/v蔗糖(pH 6.5)中,然后以0.125 g DOX/g脂質(zhì)的比例加入脂質(zhì)體。將混懸液混合并60℃加熱1小時(shí),然后在冰水中冷卻至少15分鐘。未載入的多柔比星(DOX)通過對(duì)組氨酸1.55g/L、蔗糖94g/L(pH6.5)透析(4℃)從L-DOX中分離。所得脂質(zhì)體制劑通過0.2μm注射器過濾器(聚醚砜)過濾,稀釋至2.0mg DOX?HCl/mL,并在4℃下儲(chǔ)存直至使用。
2.2.2 多柔比星脂質(zhì)體的分析
采用HPLC法測(cè)定了不同脂質(zhì)體制劑中DOX的最終濃度。在HPLC樣品制備中,用990μL甲醇加入10μL多柔比星脂質(zhì)體液相小瓶進(jìn)行稀釋。渦旋混合以破壞脂質(zhì)體并溶解脂質(zhì)體組分。配有等度泵和紫外檢測(cè)器的高效液相色譜儀(Agilent 1100)進(jìn)行分析。Zorbax eclipse XDB-C8柱(4.6 ? 150 mm, 5μm)用于分離并配備了C18反相鍵合硅膠柱(KJO-4282)和Cartridges C-8(AJO-4290),在254nm處檢測(cè)DOX。流動(dòng)相包括0.1% v/v三氟乙酸(TFA)水溶液(A)和0.1% v/v TFA甲醇溶液(B)。流動(dòng)相以1.0 mL/min的流速在12分鐘內(nèi)以40%至100%流動(dòng)相B輸送,柱溫30℃,進(jìn)樣體積為10μL。
使用等度泵、紫外可見檢測(cè)器和蒸發(fā)光散射檢測(cè)器(ELSD)HPLC(Agilent 1100)對(duì)膽固醇、磷脂和溶血素-PC濃度進(jìn)行了分析。Zorbax eclipse XDB-C8柱(4.6 ? 150 mm, 5μm)用于分離,并配備了C18反相鍵合硅膠柱(KJO-4282)和Cartridges C-8(AJO-4290)。使用紫外-可見光檢測(cè)器在205nm處檢測(cè)膽固醇,通過ELSD分析磷脂,將其設(shè)定為以下條件:蒸發(fā)器溫度為50℃,霧化器溫度為88℃,氮?dú)鈿怏w流速為1.0 L/min,光電倍增管為10,平滑度為5。高效液相色譜泵程序由以下條件組成:流動(dòng)相為0.1% TFA水溶液(A)和0.1% TFA甲醇溶液(B),在91% B下等度洗脫,流速為1.0 mL/min;進(jìn)樣體積為20μL,柱溫50℃;運(yùn)行時(shí)間30分鐘。以HSPC的mol%報(bào)告溶菌素-PC含量,定量限為HSPC的0.2mol%。使用標(biāo)準(zhǔn)磷酸鹽測(cè)定法分析脂質(zhì)體中的HSPC和PEG-DSPE含量。
使用MalvernInstruments ZetaSizer 3000HSa,通過動(dòng)態(tài)光散射測(cè)定了室溫下的平均粒徑和多分散性,Zeta平均值在表I中報(bào)告。
2.2.3 透析裝置膜的選擇
在流池法溶出儀(推薦使用華溶DS-7CP PLUS流池法溶出系統(tǒng))上裝有8-300kDa截留分子量(MWCO)的Float-a-lyzer?檢測(cè)透析管對(duì)多柔比星游離藥釋放的影響。簡(jiǎn)言之,將1.6 ml濃度為2mg/ml的游離多柔比星貯備液(在10% w/v蔗糖和10mg組氨酸/鹽酸中,pH 6.5)置于透析管中并放入流通池池體中,并使用78.4 ml 10mM組氨酸-氫氯化物(His/HCl)、5%蔗糖和0.02%NaN3(pH 6.5)作為釋放介質(zhì)(釋放介質(zhì)總體積為80ml,釋放介質(zhì)中的最終多柔比星濃度(CDOX)為40μg/ml)。流速和運(yùn)行溫度分別設(shè)定為16ml/min和37℃。一式三份測(cè)定釋放度,結(jié)果報(bào)告為平均值± SEM。
2.2.4 DOX脂質(zhì)體流池法釋放試驗(yàn)的建立
使用流池法溶出儀(推薦使用華溶DS-7CP PLUS流池法溶出系統(tǒng))檢測(cè)多柔比星的釋放。簡(jiǎn)言之,將含有1.6 mL多柔比星脂質(zhì)體樣品(0.5、1和2 mg/ml濃度的L-DOX)置于透析管中,然后放入流通池池體中。每個(gè)池體使用78.4 mL的釋放介質(zhì)。將介質(zhì)以16 ml/min的閉環(huán)系統(tǒng)灌注。
考察了釋放介質(zhì)溫度、DOX濃度和釋放介質(zhì)組成對(duì)脂質(zhì)體釋放性能的影響,試驗(yàn)建立階段在37℃、45℃和55℃下進(jìn)行釋放研究,并使用45℃的溫度選擇其他試驗(yàn)參數(shù)。在總釋放介質(zhì)中以10μg/ml、20μg/ml和40μg/ml的最終濃度進(jìn)行釋放試驗(yàn),相當(dāng)于向透析管中添加1.6 mL 0.5mg/ml、1mg/ml和2mg/ml的DOX脂質(zhì)體溶液。還考察以下因素對(duì)釋放的影響:HP-CD (1.5%、5%和20% w/v);β-CD(1.5% w/v)和γ-CD(1.5%和5% w/v)。釋放介質(zhì)中的NH4+濃度變化為0,25,50和100 mM。除非另有說明,釋放介質(zhì)中含有75 mM 2-(N-嗎啉代)乙磺酸以控制pH和0.02%NaN3作為防腐劑。釋放介質(zhì)的初始pH為6,因?yàn)榘l(fā)現(xiàn)pH6可誘導(dǎo)約50%的DOX累積釋放,這足夠根據(jù)中試研究區(qū)分不同處方。在釋放實(shí)驗(yàn)之前制備新鮮釋放介質(zhì)。
在方法開發(fā)階段,將等量游離多柔比星溶液直接置于釋放介質(zhì)中作為對(duì)照,以模擬多柔比星從脂質(zhì)體制劑中完全釋放,并監(jiān)測(cè)釋放的多柔比星在釋放期間UV吸收的任何變化。
釋放的累積百分比: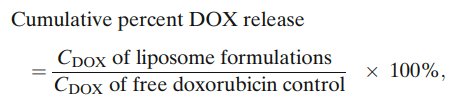
其中,脂質(zhì)體制劑的CDOX是在特定時(shí)間點(diǎn)從脂質(zhì)體釋放到釋放介質(zhì)中的多柔比星的檢測(cè)濃度,游離多柔比星對(duì)照的CDOX是在相同時(shí)間點(diǎn)的游離多柔比星的檢測(cè)濃度。在所有條件下重復(fù)測(cè)定釋放度,結(jié)果報(bào)告為平均值±SEM。
2.2.5 常規(guī)釋放試驗(yàn)
常規(guī)釋放試驗(yàn)用于研究沒有特氟龍流通池體和管的情況下DOX的釋放。簡(jiǎn)言之,將0.8 mL脂質(zhì)體制劑(CDOX=2mg/ml)置于300kDa 透析管中,隨后放入含有39.2 mL釋放介質(zhì)的50ml離心管中,總釋放介質(zhì)體積為40ml,總介質(zhì)中的最終CDOX為40μg/ml。將離心管置于轉(zhuǎn)速為320rpm/min的軌道振蕩器上,并在37℃下孵育。使用等量游離多柔比星溶液作為對(duì)照。在設(shè)定時(shí)間點(diǎn),抽取150μL釋放介質(zhì)樣品,用酶標(biāo)儀在480nm紫外線檢測(cè),并替換為等量的新鮮釋放介質(zhì)。使用早期公式計(jì)算DOX釋放的累積百分比。
2.2.6 各種脂質(zhì)體制劑DOX釋放的最終分析和檢測(cè)
最終優(yōu)化的USP-4釋放試驗(yàn)條件要求如下:(1)480 nm紫外檢測(cè);(2)截留300kda的Float-a-lyzer?透析管;(3)每次檢測(cè),將0.4 mL 2mg /mL DOX脂質(zhì)體制劑與1.2 mL釋放介質(zhì)混合,在透析管中加入共1.6 mL稀釋的脂質(zhì)體溶液(0.5 mg/mL);(4)釋放介質(zhì)78.4 mL(總介質(zhì)濃度為10 ug/mL DOX);(5)釋放介質(zhì)由5% w/v HP-CD、100 mM NH4HCO3、75 mM MES、0.02% NaN3和5% w/v蔗糖(pH 6)(簡(jiǎn)稱5% HP-CD碳酸氫銨、MES、NaN3、蔗糖(AMNS))組成;(6)流速16 mL/min;(7) 溫度45℃。
對(duì)各種DOX脂質(zhì)體制劑進(jìn)行了重復(fù)三次分析,并繪制了平均累積釋放量和SEM圖。通過f2試驗(yàn),使用以下公式評(píng)估不同處方的DOX釋放曲線之間的相似性或差異: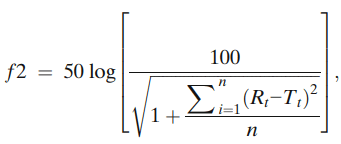
其中,n是時(shí)間點(diǎn)的數(shù)量,Rt是在時(shí)間t(t > 0)的參比批次的累積釋放值,Tt是測(cè)試批次在時(shí)間t(t > 0)的累積釋放值。所有時(shí)間點(diǎn)的累積釋放值(n=24)用于計(jì)算f2。相似系數(shù)f2 ≥50被認(rèn)為與參比處方相似。
為了確定每天的變異性,在三個(gè)不同的日期分析相同的樣品;每天重復(fù)三次。報(bào)告了7小時(shí)和24小時(shí)多柔比星累積釋放的平均值、SEM和方差。還計(jì)算并報(bào)告了f2。
3.1 多柔比星脂質(zhì)體的制備與表征
制備了組成與Doxil?相同的脂質(zhì)體制劑,并對(duì)其進(jìn)行了表征,用于流池法藥物釋放試驗(yàn)開發(fā)。在表I中總結(jié)了組成、制備脂質(zhì)體所用的方法及其分析特性的差異。脂質(zhì)體的平均大小和多分散性指數(shù)(PDI)通過DLS測(cè)量,并且在表I中報(bào)告了Zeta平均值。通過不同HPLC方法測(cè)定了脂質(zhì)體的多柔比星、溶血素-PC和膽固醇含量。用標(biāo)準(zhǔn)磷酸鹽測(cè)定法測(cè)定磷脂含量或HSPC和DSPE-PEG2000的總和。總脂是磷脂和膽固醇含量的算術(shù)均值(表1)。
L- DOXp和L-DOXi的MLV制備方法有所不同。L-DOXP為將含脂乙醇溶液倒入攪拌下的硫酸銨水溶液中,L-DOXi為高壓注入。雖然L-DOXi和L-DOXp的平均尺寸和多分散性非常相似,但L-DOXp釋放DOX速度更慢,如下文所述。為了進(jìn)一步研究生產(chǎn)工藝對(duì)多柔比星釋放的影響,我們采用均質(zhì)法制備了脂質(zhì)體。與擠出制備的脂質(zhì)體相比,所得脂質(zhì)體的平均粒徑略小,PDI更高。通過均質(zhì)制備的脂質(zhì)體釋放DOX比擠出制備的脂質(zhì)體更快。為了研究流池法試驗(yàn)是否能夠區(qū)分緩釋和快速釋放制劑,我們用等量的POPC取代HSPC制備了脂質(zhì)體。POPC熔融溫度(-2℃)比HSPC(53℃)低,因此預(yù)計(jì)DOX會(huì)更快釋放。雖然HSPC替代POPC略微改變了脂質(zhì)與DOX的摩爾比,但質(zhì)量比保持不變。
3.2 透析裝置膜的選擇
透析袋/透析管可用作屏障,使釋放的多柔比星快速擴(kuò)散到釋放介質(zhì)中,同時(shí)保留仍包封在脂質(zhì)體中的所有多柔比星。為了找到能夠滿足這一要求的特定透析袋/管膜,通過在透析袋中直接添加游離多柔比星溶液來測(cè)試具有不同MWCO和材料的膜,以模擬所有藥物分子從脂質(zhì)體中釋放的條件。
結(jié)果表明,采用100-300kDa MWCO的Float-a-lyzer?CE膜可快速釋放多柔比星,在37℃下的7h內(nèi)釋放幾乎100%的多柔比星,而采用8-10kDa MWCO的膜在24h內(nèi)僅觀察到33.9% ±2.2%的累積釋放(見圖1),100和300kDa MWCO膜的DOX轉(zhuǎn)運(yùn)速率無顯著差異,因此所有后續(xù)研究均使用300kDa MWCO膜。100-300kDa MWCO膜的孔徑范圍為5-8nm,比我們的脂質(zhì)體粒徑小得多。因此,仍包封在脂質(zhì)體中的多柔比星不會(huì)穿過膜。此外,釋放24小時(shí)后,在釋放介質(zhì)中未檢測(cè)到脂質(zhì)體,HPLC檢測(cè)沒有磷脂即可證明這一點(diǎn)。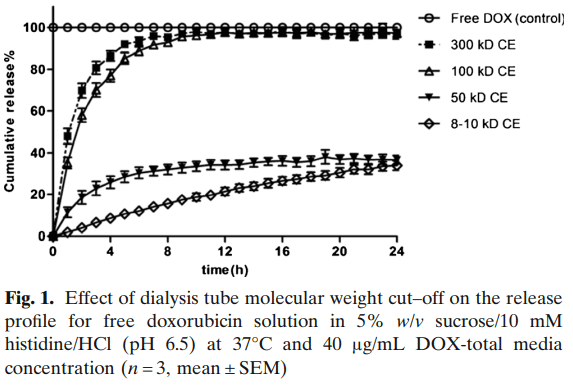
3.3 多柔比星釋放試驗(yàn)初步開發(fā)
3.3.1 解決釋放介質(zhì)中的DOX沉淀問題
在確定了游離多柔比星的適當(dāng)透析膜后,在SOTAX ?流池法溶出儀上進(jìn)行了多柔比星從脂質(zhì)體的釋放試驗(yàn)。建立了游離DOX溶液在各種釋放介質(zhì)中0-45μg/ml的標(biāo)準(zhǔn)曲線,包括10mM His/HCl和5%蔗糖(pH=6.5)、PBS(pH=7.4)和100 mM NH4HCO3/5%蔗糖(pH 6.0)。使用進(jìn)化陣列紫外可見分光光度計(jì)480nm檢測(cè)DOX,并在0-45μg/mL濃度范圍內(nèi)觀察到所有介質(zhì)的良好線性。初步藥物釋放,在介質(zhì)100mM NH4HCO3(5% 蔗糖,pH6)(圖2a)或PBS(pH7)中以40μg/mL總DOX濃度進(jìn)行實(shí)驗(yàn),意外的是,在SOTAX ?流池法溶出儀的兩種介質(zhì)中均觀察到DOX沉淀。進(jìn)一步的研究表明,溶出儀的聚四氟乙烯表面形成了較小的紅色晶體,隨著時(shí)間的推移,其尺寸逐漸增大,最終導(dǎo)致多柔比星沉淀。為了探索儀器特氟隆表面或釋放介質(zhì)中的有限D(zhuǎn)OX溶解度是否為藥物沉淀的原因,在聚丙烯離心管中進(jìn)行釋放(參見常規(guī)釋放試驗(yàn)) 。在無聚四氟乙烯條件下,DOX沉淀的程度也較小。在離心管中加入特氟隆攪拌棒時(shí),即使在DOX濃度低至3μg/ml下,也觀察到在特氟隆表面上形成紅色沉淀。為了避免在流池法溶出儀系統(tǒng)中釋放期間沉淀,我們將羥丙基環(huán)糊精(HP-CD)作為DOX溶解度增強(qiáng)劑添加到釋放介質(zhì)中。
添加1.5%、5%和20%時(shí),HP-CD可提高DOX在釋放介質(zhì)中的溶解度。在向釋放介質(zhì)中添加HP-CD之前和之后,使用常規(guī)測(cè)定進(jìn)行釋放研究,48小時(shí)內(nèi)未觀察到DOX沉淀。在常規(guī)分析中添加特氟龍表面并在介質(zhì)中加入HP-CD不會(huì)導(dǎo)致多柔比星沉淀(圖2b)。初始釋放實(shí)驗(yàn)在37℃下于PBS,10mM his/HCl緩沖液或100mM NH4HCO3中進(jìn)行,然而,僅在NH4HCO3緩沖液中觀察到脂質(zhì)體釋放DOX。此外,DOX釋放百分比在pH5-7之間高度依賴于NH4HCO3溶液pH。發(fā)現(xiàn)pH6 介質(zhì)在24小時(shí)內(nèi)誘導(dǎo)DOX的累積釋放約50%,這足以區(qū)分基于中試研究的不同處方。然而,在37℃下釋放DOX期間,100mM NH4HCO3/5% w/v蔗糖介質(zhì)的pH從6增加至8,導(dǎo)致多柔比星的紫外吸收降低,這降低了分析準(zhǔn)確度。此外,在含蔗糖的介質(zhì)中觀察到細(xì)菌生長(zhǎng)。為避免pH在釋放過程中增加,在釋放介質(zhì)中加入緩沖至pH6.0的75mM MES。在釋放介質(zhì)中加入75mM MES后,pH的變化非常適中,37℃下48h后,pH由6增加至6.2,DOX紫外吸收保持不變。向釋放介質(zhì)中添加防腐劑0.02% w/v NaN3可防止細(xì)菌生長(zhǎng)。因此,我們選擇了含NH4HCO3、MES和NaN3的釋放介質(zhì)進(jìn)行進(jìn)一步評(píng)估。我們將此介質(zhì)縮寫為“AMNS”(碳酸氫銨、MES、NaN3、蔗糖)。然而,即使在存在100mM NH4HCO3的情況下,通過常規(guī)釋放試驗(yàn)(圖2b),在37℃下24小時(shí)內(nèi)DOX的釋放程度有限僅約7%,因此需要探索增加釋放速率的額外措施。隨后進(jìn)行的實(shí)驗(yàn)考察溶出系統(tǒng)溫度對(duì)其釋放的影響。
3.3.2 流池溶出系統(tǒng)溫度對(duì)DOX釋放的影響
多柔比星的釋放與溫度高度相關(guān),7小時(shí)內(nèi)多柔比星累積釋放百分比為91.0%±1.6%、42.4%±0.6%和4.5%±0.1%的試驗(yàn)溫度分別為55℃、45℃、37℃(圖2c)。DOX脂質(zhì)體主要組分HSPC的凝膠-液晶相變溫度(Tm)為53 ℃。當(dāng)溫度高于Tm時(shí),釋放量顯著增加,這不足為奇。選擇45℃的溫度進(jìn)行后續(xù)研究,因?yàn)長(zhǎng)-DOXi的累積釋放百分比幾乎在24小時(shí)內(nèi)就可以釋放完全(95.3% ±1.2%),但釋放速率足夠慢,可以區(qū)分處方之間的差異。
3.3.3 流池法溶出儀釋放試驗(yàn)的優(yōu)化
3.3.3.1 不同濃度L-D0X對(duì)DOX釋放的影響
考察了L-DOX制劑與總釋放介質(zhì)的體積比對(duì)流池法中DOX釋放速率的影響。L-DOX的標(biāo)準(zhǔn)濃度為2mg/ml。將L-DOX稀釋至0.5、1和2mg/ml的濃度,并將1.6ml稀釋的L-DOX置于Float-a-lyzer?透析管中,將透析管插入流通池體中,并向每個(gè)釋放管路中添加78.4ml的釋放介質(zhì)。因此,100%的多柔比星釋放會(huì)在總釋放介質(zhì)中產(chǎn)生10μg/ml、20μg/ml和40μg/ml的藥物濃度。初始L-DOX濃度越低,多柔比星累積釋放越高:分別在24h內(nèi)釋放了77.0% ±2.7%、60.9% ±0.6%和48.3 ±0.7%的mL(圖3a),由于多柔比星檢測(cè)最低濃度是精確的儀器中的濃度和多柔比星沉淀風(fēng)險(xiǎn)在最低濃度下較低,所有后續(xù)研究均使用總介質(zhì)中的10μg/ml的多柔比星濃度(透析管中多柔比星濃度為0.5mg/ml)。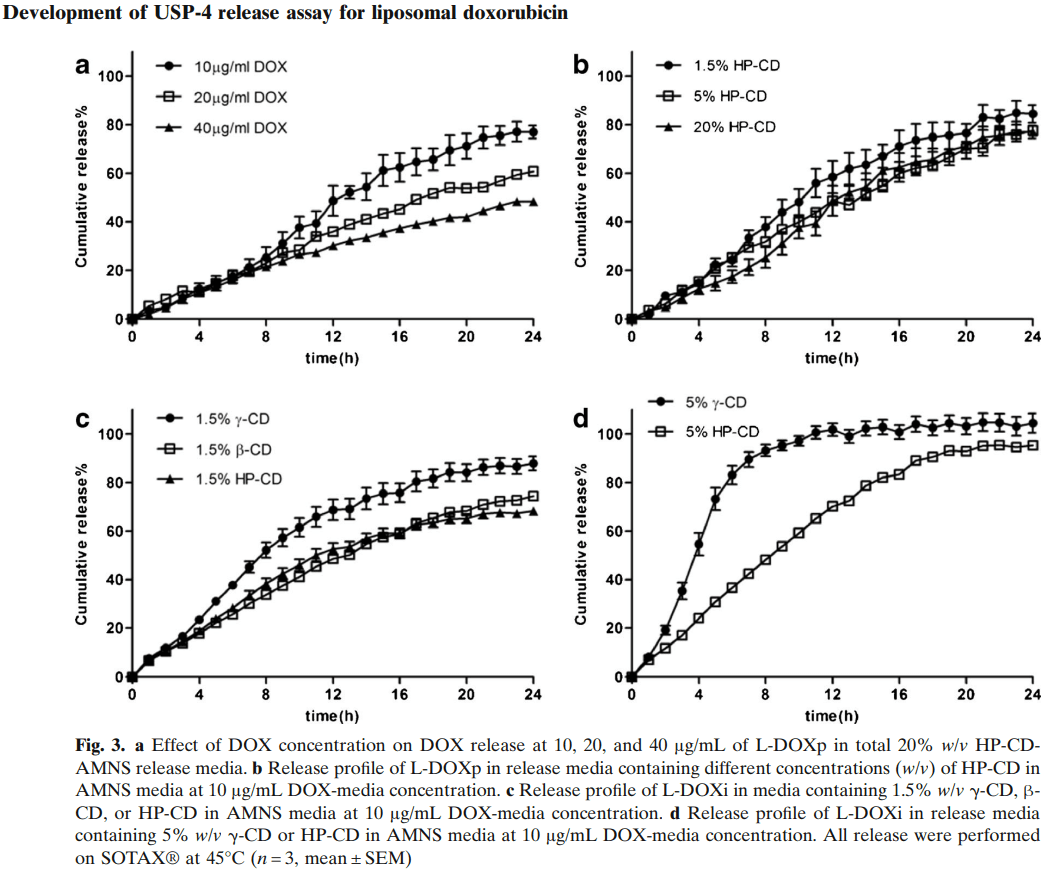
3.3.3.2 環(huán)糊精類型和濃度對(duì)DOX釋放的影響
考察釋放介質(zhì)中HP-CD濃度對(duì)DOX釋放的影響。含1.5%、5%和20% HP-CD的釋放介質(zhì)的累積藥物釋放沒有顯著差異(對(duì)于1.5%的HP-CD和5%的HP-CD,f2為53.1;對(duì)于1.5%的HP-CD和20%的HP-CD,f2為52.7;對(duì)于5%的HP-CD和20%的HP-CD,f2為68.7)(圖3b),在含有5%和20% HP-CD的釋放介質(zhì)中未檢測(cè)到多柔比星沉淀,但在使用1.5%HP-CD時(shí)出現(xiàn)微量沉淀。
為了比較環(huán)糊精類型對(duì)DOX釋放的影響,將1.5%γ-CD、β-CD或HP-CD添加到含有100mM NH4HCO3、75mM MES、5%蔗糖和0.02%NaN3的釋放介質(zhì)中。由于β-CD的水溶性有限,實(shí)驗(yàn)在1.5%環(huán)糊精介質(zhì)濃度下進(jìn)行。與HP-CD和β-CD相比,γ-CD的DOX釋放更快(圖3c)。不幸的是,當(dāng)三種環(huán)糊精僅在1.5%濃度下使用時(shí),都觀察到DOX的微量沉淀。為了避免DOX沉淀,對(duì)含有5%γ-CD和HP-CD介質(zhì)的藥物釋放進(jìn)行了研究。在含5%γ-CD介質(zhì)中,在7小時(shí)DOX累積釋放為89.5% ±3.1%,而含5%HP-CD介質(zhì)中的累積釋放為42.4% ±0.6%(圖3d)。對(duì)于5%γ-CD釋放介質(zhì),DOX釋放太快,可能會(huì)降低區(qū)分不同L-DOX制劑的能力。此外,與HP-CD相比,γ-CD輔料成本更高,因此在釋放試驗(yàn)中使用γ-CD是不切實(shí)際的。因此,在優(yōu)化的釋放試驗(yàn)中使用了5%HP-CD。
3.3.3.3 NH4+對(duì)多柔比星釋放的影響
在流池法溶出儀上研究了釋放介質(zhì)中NH+濃度對(duì)DOX釋放速率的影響。NH4HCO3釋放介質(zhì)濃度對(duì)DOX釋放有顯著影響(圖4),在沒有NH4HCO3的情況下,DOX釋放非常有限,釋放速率隨NH4HCO3濃度的增加而增加。因此,100mM NH4HCO3釋放介質(zhì)用于后續(xù)研究。
根據(jù)實(shí)驗(yàn)結(jié)果,確定了DOX脂質(zhì)體的流通池法釋放試驗(yàn)方法。優(yōu)化后的釋放介質(zhì)組成為100mM NH4HCO3、75mM MES和5%HP-CD、5%蔗糖和0.02%NaN3(pH6)。在45℃下以16ml/min的速度循環(huán)釋放介質(zhì),24小時(shí)檢測(cè)DOX釋放,釋放介質(zhì)體積為80ml,總釋放介質(zhì)中DOX的最終濃度為10μg/ml,相當(dāng)于向透析管(Float-a-lyzer?)中添加1.6ml濃度為0.5mg/ml的DOX脂質(zhì)體。
3.3.3.4 釋放試驗(yàn)的有限確認(rèn)
通過使用相同的L-DOXi制劑在三個(gè)不同的日期運(yùn)行釋放試驗(yàn),通過前述優(yōu)化的流池法溶出儀進(jìn)行釋放試驗(yàn),分析了日間變異性。7小時(shí)和24小時(shí)的累積釋放量分別為47.0%±1.6%和96.5%±0.7%,表明測(cè)定方差有限,釋放曲線無顯著差異(第1天和第2天的f2為73.4,第1天和第3天的f2為63.4,第2天和第3天的f2為81.0)(圖5),對(duì)照DOX溶液的UV強(qiáng)度變化在四個(gè)不同的日期進(jìn)行評(píng)估。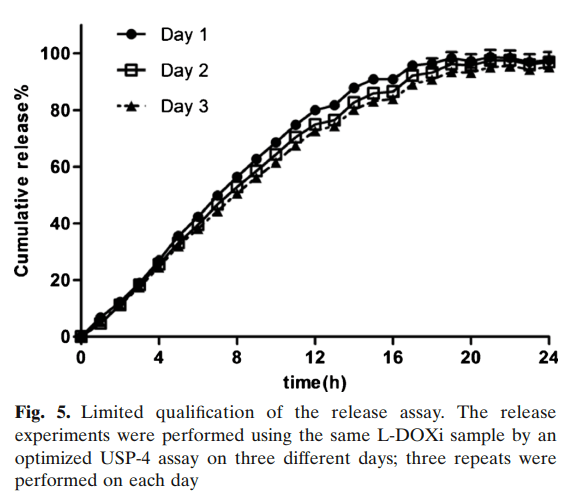
3.3.3.5 脂質(zhì)體組成和制備方法對(duì)DOX釋放的影響
為驗(yàn)證已建立的流池法釋放試驗(yàn)區(qū)分DOX釋放的能力,檢查了各種脂質(zhì)體制劑的差異(圖6)。將市售的Doxil?作為對(duì)照進(jìn)行分析。用POPC替代HSPC可在10小時(shí)內(nèi)快速完全釋放DOX(圖6a)。所有其他脂質(zhì)體的組成與Doxil?相同,但其理化性質(zhì)略有不同。通過f2計(jì)算定量評(píng)估了這些處方之間的DOX釋放差異(表2)。當(dāng)f2值大于50時(shí),認(rèn)為兩種處方的釋放曲線相似。在表2中列出的多項(xiàng)比較中,這些比較的f2值小于50,并且認(rèn)為它們的DOX釋放行為彼此不同。

我們制備的所有制劑的DOX釋放速率均低于市售Doxil?。在制備的脂質(zhì)體中,使用高壓均質(zhì)(H-DOX)制備的脂質(zhì)體比L-DOXp表現(xiàn)出更快的釋放速率,24小時(shí)累積釋放分別為82.9%±0.3%和77.7%±1.3%(圖6a)。與L-DOXp平均粒徑為91.0±0.1 nm相比,H-DOX(79.4±0.3 nm)的平均粒徑更小,粒徑分布更寬。H-DOX粒徑的非均勻性可以解釋DOX釋放速率的加快。
在脂質(zhì)體擠出之前制備MLV的方法也對(duì)DOX釋放有影響。在硫酸銨水溶液中倒入脂質(zhì)溶液制備的MLVs(L-DOXp)的DOX釋放比在水溶液中高壓注入脂質(zhì)溶液制備的MLV(L-DOXi)要慢。此外,釋放介質(zhì)中存在環(huán)糊精和NH4HCO3不會(huì)導(dǎo)致以顆粒粒徑發(fā)生劇烈變化為特征的脂質(zhì)體崩解。在釋放過程中,脂質(zhì)體保持完整,并且僅進(jìn)行了有限的顆粒尺寸增加(表2)。
選擇釋放介質(zhì)是成功開發(fā)流池法釋放試驗(yàn)的關(guān)鍵。雖然低離子強(qiáng)度介質(zhì)10% 蔗糖和10mM his/HCl(pH 6.5)可以很好的溶解游離多柔比星,且不會(huì)引起明顯沉淀,但該釋放介質(zhì)不能誘導(dǎo)多柔比星從脂質(zhì)體中釋放。同樣,單獨(dú)使用PBS也不會(huì)誘導(dǎo)多柔比星釋放。近年來,有報(bào)道稱腫瘤細(xì)胞可以通過谷氨酰胺分解產(chǎn)生氨,并誘導(dǎo)多柔比星從脂質(zhì)體中釋放出來。我們的初步研究還發(fā)現(xiàn),當(dāng)添加NH4+到釋放介質(zhì)中時(shí),多柔比星的累積釋放顯著增加。此外,脂質(zhì)體釋放的多柔比星高度依賴于釋放介質(zhì)的pH和NH4+濃度。在100mM的相同NH4+濃度下,當(dāng)釋放介質(zhì)的pH從4.5增加到7.0時(shí),脂質(zhì)體釋放的多柔比星累積百分比從0%增加到80%, 同樣,當(dāng)釋放介質(zhì)中的NH4+濃度從0增加到100mM時(shí),多柔比星累積釋放百分比也會(huì)增加,這并不奇怪,因?yàn)槎嗳岜刃峭ㄟ^硫酸銨梯度法被加載到脂質(zhì)體中,并且多柔比星可以在脂質(zhì)體內(nèi)硫酸鹽存在下形成晶體。多柔比星作為游離有機(jī)堿,對(duì)脂質(zhì)體的脂質(zhì)雙分子層具有高滲透性,但當(dāng)其質(zhì)子化并因此被捕獲在脂質(zhì)體內(nèi)時(shí),則具有低滲透性。氨鹽在釋放介質(zhì)中pH依賴性分解后,NH3能夠穿透脂質(zhì)體膜,去質(zhì)子化多柔比星,并促進(jìn)其通過脂質(zhì)膜的轉(zhuǎn)運(yùn),當(dāng)氨在增加pH被中和時(shí),釋放介質(zhì)中的氨變得更通透。因此,較高的pH和較高的NH4+濃度可誘導(dǎo)更多的多柔比星釋放。
然而,當(dāng)使用含NH4+的釋放介質(zhì)進(jìn)行釋放測(cè)定時(shí),多柔比星會(huì)沉淀在流通池體和特氟隆管路,即使在低至3μg/ml的多柔比星濃度下,聚四氟乙烯的管路也會(huì)導(dǎo)致沉淀。為了避免釋放的多柔比星沉淀,HP-CD可以通過將客體分子封裝在空腔中,將其溶解到釋放介質(zhì)中,因此,添加HP-CD后未發(fā)生沉淀。然而,在釋放介質(zhì)中使用環(huán)糊精通過不同的機(jī)制增強(qiáng)了多柔比星釋放,環(huán)糊精能夠從脂質(zhì)體膜中提取膽固醇,從而提高膜的流動(dòng)性和通透性。24小時(shí)釋放研究完成后,對(duì)脂質(zhì)體中殘留膽固醇含量的HPLC分析以及釋放介質(zhì)的分析證實(shí),有30%的膽固醇離開脂質(zhì)體,并在5%HP-CD釋放介質(zhì)中也有發(fā)現(xiàn)。在血漿中,可能發(fā)生與循環(huán)脂蛋白從注射的脂質(zhì)體中提取膽固醇類似的事件。
解決沉淀問題后,進(jìn)一步優(yōu)化該釋放試驗(yàn),以便在24小時(shí)內(nèi)幾乎完全釋放多柔比星,從而提高試驗(yàn)的區(qū)分能力,因而評(píng)估了釋放介質(zhì)中的多柔比星濃度、釋放介質(zhì)組成以及溫度的影響。溫度越高,多柔比星釋放速率越快,這并不奇怪,因?yàn)樵诟叩臏囟认拢さ牧鲃?dòng)性越高,膜的流動(dòng)性有助于銨離子進(jìn)入脂質(zhì)體,多柔比星從脂質(zhì)體中擴(kuò)散出來,以及環(huán)糊精提取膽固醇。此外,在較高的溫度下,NH3的生成速率較高,有效的多柔比星溶解度、擴(kuò)散和解離常數(shù)較高,從而加快了分子的遷移和反應(yīng)性。然而,過高的釋放速率(55℃)或過低的釋放速率(37℃)可能會(huì)掩蓋不同制劑之間的任何輕微差異,因此,使用中等釋放速率(45℃)作為釋放試驗(yàn)的溫度,這為區(qū)分不同制劑提供了更好的機(jī)會(huì)。
流池法測(cè)定的主要局限性在于測(cè)定條件本身確定了脂質(zhì)體釋放多柔比星的驅(qū)動(dòng)力。因此,該試驗(yàn)可主要用于確定多柔比星脂質(zhì)體制劑之間的相對(duì)差異,而不是確定體內(nèi)相關(guān)釋放行為。似乎NH4HCO3的存在和pH依賴性形成是溶解和釋放多柔比星的關(guān)鍵驅(qū)動(dòng)力。即使所有其他參數(shù)(如HP-CD和高溫)保持不變,在小于25 mM NH4HCO3時(shí)觀察到幾乎沒有多柔比星釋放(圖4)。L-DOX濃度分別為10μg/ml、20μg/ml和40μg/ml時(shí),加快的多柔比星釋放速率降低,這也歸因于多柔比星-硫酸鹽溶出期間透析管內(nèi)NH4HCO3與多柔比星脂質(zhì)體的比率較高和瞬態(tài)pH變化。雖然可以使用相同數(shù)量的NH3溶解多柔比星脂質(zhì)體,但隨后,它會(huì)溶解較高比例的總多柔比星,從而導(dǎo)致更完全的藥物釋放。
溫度對(duì)釋放速率也有明顯的影響(圖2c)。在含有HP-CD、MES和100 mM NH4HCO3的所有相同介質(zhì)中,在37℃下幾乎沒有觀察到多柔比星釋放,在55℃下快速且?guī)缀跞康乃幬镝尫旁?h內(nèi)達(dá)到平臺(tái),與在45℃下持續(xù)釋放多柔比星形成對(duì)比。在55℃下,脂質(zhì)體膜類似流體,因此多柔比星可以通過膜快速擴(kuò)散,釋放介質(zhì)中HP-CD的存在有助于去除脂質(zhì)膜中的膽固醇,減少膜的有效過渡,并提高多柔比星滲透性。顯然,試驗(yàn)溫度顯著影響多柔比星的有效釋放速率,最終選擇的流池法參數(shù)與生理?xiàng)l件相差甚遠(yuǎn)。然而,加速釋放條件已被其他研究者用于建立基于流池法的聚合物微球評(píng)估方法。在流池法試驗(yàn)中,使用pH2.4的極端釋放介質(zhì)pH、添加10% 乙醇以及45℃、50℃、53℃和60℃的高溫來區(qū)分聚合物微球處方。
除釋放介質(zhì)組成和溫度外,流池法釋放裝置的設(shè)置本身也會(huì)影響多柔比星釋放。為了檢測(cè)脂質(zhì)體的藥物釋放,我們使用了透析裝置插入U(xiǎn)SP-4裝置。我們發(fā)現(xiàn),透析膜代表了多柔比星從Float-a-lyzer ?擴(kuò)散到USP-4流通池的擴(kuò)散屏障,值得注意的是,高滲透性300 kDa透析管的釋放存在滯后時(shí)間,這使我們對(duì)釋放動(dòng)力學(xué)的有效觀察延遲了大約1小時(shí)(圖1中50%釋放的時(shí)間約為1小時(shí))。因此,由于脂質(zhì)體制劑的釋放是在更長(zhǎng)的時(shí)間尺度上觀察到的(例如,半時(shí)間約7小時(shí)),我們正在觀察藥物從脂質(zhì)體釋放的動(dòng)力學(xué)有價(jià)值的表現(xiàn)(圖5)。然而,使用其他滲透率較低的50-10kDa透析膜會(huì)導(dǎo)致多柔比星溶液從Float-a-lyzer?中釋放顯著減慢和不完全釋放。這種影響可能取決于藥物的大小和疏水性,因此,對(duì)于難溶、分子量較大的藥物,這種影響可能更為嚴(yán)重。
選擇用于分析的最終條件與L-DOX的生理釋放條件相去甚遠(yuǎn)。USP-4試驗(yàn)條件的主要優(yōu)化標(biāo)準(zhǔn)是在12小時(shí)內(nèi)從Doxil?中觀察到超過80%的藥物釋放,以便能夠在試驗(yàn)持續(xù)時(shí)間的24小時(shí)內(nèi)區(qū)分具有更快或更慢多柔比星釋放行為的脂質(zhì)體制劑。實(shí)際上,當(dāng)使用優(yōu)化的釋放試驗(yàn)來確定不同L-DOX制劑的釋放曲線時(shí),它能夠區(qū)分慢釋放和快釋放脂質(zhì)體制劑。例如,POPC L-DOX的釋放速率比任何其他制劑都快,在10h內(nèi)釋放幾乎100%的多柔比星。這并不奇怪,因?yàn)镻OPC的相變溫度遠(yuǎn)低于其他脂質(zhì)體制劑。相變溫度較低的磷脂具有較高的流動(dòng)性,這使得分子更容易通過脂質(zhì)雙層運(yùn)輸。我們還發(fā)現(xiàn),組成相同但通過不同方法制備的制劑,以及具有略微不同理化性質(zhì)的制劑,在體外表現(xiàn)出非常不同的釋放,均質(zhì)脂質(zhì)體具有更寬的粒徑分布(表1),與擠出制備的脂質(zhì)體相比,多柔比星釋放更快。通過均質(zhì)化縮小MLVs粒徑的工藝不能實(shí)現(xiàn)與擠出相同的粒徑控制。脂質(zhì)體粒徑分布越大,某些脂質(zhì)體的釋放速率越快。MLV制備方法似乎對(duì)多柔比星釋放速率有很大影響,因?yàn)長(zhǎng)-DOXi的藥物釋放比L-DOXp快。脂類或硫酸銨的層狀排列可能存在差異,有些脂質(zhì)體或小粒徑非均勻性低于DLS檢測(cè)能力,需要通過對(duì)不同脂質(zhì)體的顯微鏡分析進(jìn)一步解釋這種差異。
雖然未進(jìn)行正式的分析驗(yàn)證,但有限的確認(rèn)顯示,在不同日期(圖5)對(duì)同一L-DOX制劑進(jìn)行的分析變異性較低,多柔比星溶液對(duì)照信號(hào)強(qiáng)度的日間變異性較低。然而,我們發(fā)現(xiàn)多柔比星釋放速率強(qiáng)烈依賴于NH4HCO3溶液的離子強(qiáng)度和介質(zhì)的初始pH。這可能與藥物非臨床試驗(yàn)質(zhì)量管理規(guī)范(GLP)的含量驗(yàn)證存在潛在問題,因此,可能需要進(jìn)一步優(yōu)化氨鹽濃度和pH,以提高分析耐用性。此外,在每次USP-4儀器運(yùn)行中使用L-DOX標(biāo)準(zhǔn)制劑作為對(duì)照,并以與對(duì)照的百分比差異表示釋放度結(jié)果,這可以在GLP分析驗(yàn)證中實(shí)施。
我們研究中采用的設(shè)計(jì)原理和選擇適當(dāng)釋放條件的方法可能是開發(fā)其他通用復(fù)合脂質(zhì)體制劑分析的有用范例。
使用含100 mM NH4HCO3、5%蔗糖、75mM MES、0.02%NaN3和5%HP-CD的釋放介質(zhì),在45℃下用流池法溶出儀進(jìn)行24小時(shí)的多柔比星脂質(zhì)體釋放試驗(yàn)。該釋放試驗(yàn)用于區(qū)分不同工藝制備的相似多柔比星脂質(zhì)體的差異。已建立的流池法試驗(yàn)可用于區(qū)分原研和仿制多柔比星脂質(zhì)體之間的可能差異,為設(shè)計(jì)更好的制劑提供有用的反饋,并可能將這些制劑的體外釋放行為與體內(nèi)藥代動(dòng)力學(xué)聯(lián)系起來。
略
如需原文,請(qǐng)聯(lián)系小編 (代老師15012941165)